Voorafgaande aan behandeling biologicals
Het onderwerp 'voorafgaande aan de behandeling met biologicals' is uitgewerkt in submodules.
Onderbouwing
Referenties
- Askling J, Fored CM, Baecklund E, Brandt L, Backlin C, Ekbom A et al. Haematopoietic malignancies in rheumatoid arthritis: lymphoma risk and characteristics after exposure to tumour necrosis factor antagonists. Ann Rheum Dis. 2005;64:1414-20.
- Askling J, Baecklund E, Granath F, Geborek P, Fored M, Backlin C et al. Anti-tumour necrosis factor therapy in rheumatoid arthritis and risk of malignant lymphomas: relative risks and time trends in the Swedish Biologics Register. Ann Rheum Dis. 2009;68:648-53.
- Askling J, van Vollenhoven RF, Granath F, Raaschou P, Fored CM, Baecklund E et al. Cancer risk in patients with rheumatoid arthritis treated with anti-tumor necrosis factor alpha therapies: does the risk change with the time since start of treatment? Arthritis Rheum. 2009;60:3180-3189.
- Assen van S, Hovast A, et al. Humoral responses after influenza-vaccination are severely reduced in patients with rheumatoid arthritis treated with rituximab. Ann Rheum Dis 2009;68(Suppl3):567.
- Augustsson J, Eksborg S, Ernestam S, Gullstrom E, van Vollenhoven R. Low-dose glucocorticoid therapy decreases risk for treatment-limiting infusion reaction to infliximab in patients with rheumatoid arthritis. Ann Rheum Dis 2007; 66(11):1462-6.
- Appau et al J Gastrointest Surg. 2008;12:1738-44.
- Baert F, Noman M, Vermeire S, Van Assche G, D' Haens G, Carbonez A et al. Influence of immunogenicity on the long-term efficacy of infliximab in Crohn's disease. N Engl J Med 2003; 348(7):601-8.
- Bartelds GM, Wolbink GJ, Stapel S, Aarden L, Lems WF, Dijkmans BA et al. High levels of human anti-human antibodies to adalimumab in a patient not responding to adalimumab treatment. Ann Rheum Dis 2006; 65(9):1249-50.
- Bartelds GM, Wijbrandts CA, Nurmohamed MT, Stapel S, Lems WF, Aarden L et al. Clinical response to adalimumab: relationship to anti-adalimumab antibodies and serum adalimumab concentrations in rheumatoid arthritis. Ann Rheum Dis 2007; 66(7):921-6.
- Beaugerie L, Brousse N, Bouvier AM, Colombel JF, Lemann M, Cosnes J et al. Lymphoproliferative disorders in patients receiving thiopurines for inflammatory bowel disease: a prospective observational cohort study. Lancet. 2009;374:1617-25.
- Berger CT, Recher M, Steiner U, Hauser TM. A patients wish: anakinra in pregnancy. Ann Rheum Dis 2009; 68: 1794-5.
- Bernatsky S, Hudson M, Suissa S. Anti-rheumatic drug use and risk of hospitalization for congestive heart failure in rheumatoid arthritis. Rheumatology (Oxford) 2005; 44(5):677-80.
- Bernstein CN, Blanchard JF, Kliewer E, Wajda A. Cancer risk in patients with inflammatory bowel disease: a population-based study. Cancer. 2001;91:854-62.
- Biancone L, Calabrese E, Petruzziello C, Pallone F. Treatment with biologic therapies and the risk of cancer in patients with IBD. Nat Clin Pract Gastroenterol Hepatol. 2007;4:78-91.
- Bibbo C, Goldberg JW. Infectious and healing complications after elective orthopaedic foot and ankle surgery during tumor necrosis factor-alpha inhibition therapy.
- Bijl, van der AE, Breedveld FC, Antoni CE, Kalden JR, Kary S, Burmester GR et al. An open-label pilot study of the effectiveness of adalimumab in patients with rheumatoid arthritis and previous infliximab treatment: relationship to reasons for failure and anti-infliximab antibody status. Clin Rheumatol 2008; 27(8):1021-8.
- Blonski W, Lichtenstein GR. Safety of biologic therapy. Inflamm Bowel Dis 2007; 13: 769-96.
- Bongartz T, Sutton AJ, Sweeting MJ, Buchan I, Matteson EL, Montori V. Anti-TNF antibody therapy in rheumatoid arthritis and the risk of serious infections and malignancies: systematic review and meta-analysis of rare harmful effects in randomized controlled trials. JAMA 2006; 295(19):2275-85.
- Braun et al, ARD 2006
- Bresnihan B. The safety and efficacy of interleukin-1 receptor antagonist in the treatment of rheumatoid arthritis. Semin Arthritis Rheum 2001; 30(5 Suppl 2):17-20.
- Bresnihan B, Newmark R, Robbins S, Genant HK. Effects of anakinra monotherapy on joint damage in patients with rheumatoid arthritis. Extension of a 24-week randomized, placebo-controlled trial. J Rheumatol 2004; 31(6):1103-11.
- Brimhall AK, King LN, Licciardone JC, Jacobe H, Menter A. Safety and efficacy of alefacept, efalizumab, etanercept and infliximab in treating moderate to severe plaque psoriasis: a meta-analysis of randomized controlled trials. Br J Dermatol 2008; 159(2):274-85.
- Callegari PE, Schaible TF, Boscia JA. Risk of serious infections and malignancies with anti-TNF antibody therapy in rheumatoid arthritis. JAMA 2006; 296(18):2202-4.
- Campi P, Benucci M, Manfredi M, Demoly P. Hypersensitivity reactions to biological agents with special emphasis on tumor necrosis factor-alpha antagonists. Curr Opin Allergy Clin Immunol 2007; 7(5):393-403.
- Carmona L, Gomez-Reino JJ, Rodriguez-Valverde V, Montero D, Pascual-Gomez E, Mola EM et al. Effectiveness of recommendations to prevent reactivation of latent tuberculosis infection in patients treated with tumor necrosis factor antagonists. Arthritis Rheum 2005; 52(6):1766-72.
- Carmona L, Descalzo MA, Perez-Pampin E, Ruiz-Montesinos D, Erra A, Cobo T et al. All-cause and cause-specific mortality in rheumatoid arthritis are not greater than expected when treated with tumour necrosis factor antagonists. Ann Rheum Dis 2007; 66(7):880-5.
- Carter JD, Valeriano J, Vassey FB. Tumor necrosis factor-a inhibition and VATER association: a causal relationship? J Rheumatol 2006; 33: 1014-7.
- Carter JD, Ladhani A, Ricca L, et al A safety assessment of TNF antagonists during pregnancy: a review of the FDA database [abstract] Arthritis & Rheum 2007; 56 (Suppl): S286-7.
- Carter JD, Ladhani A, Ricca LR, Valeriano J, Vasey FB. A safety assessment of tumor necrosis factor antagonists during pregnancy: a review of the Food and Drug Administration database. J Rheumatol 2009; 36: 635-41.
- Cauza E, Cauza K, Hanusch-Enserer U, Etemad M, Dunky A, Kostner K. Intravenous anti TNF-alpha antibody therapy leads to elevated triglyceride and reduced HDL-cholesterol levels in patients with rheumatoid and psoriatic arthritis. Wien Klin Wochenschr 2002; 114(23-24):1004-7.
- Chakravarty EF, Sanchez-Yamamoto D, Bush TE. The use of disease modifying anti-rheumatic drugs in women with rheumatoid arthritis of child bearing age: a survey of practice patters and pregnancy outcomes. J Rheum 2003; 30: 241-6.
- Chakravarty EF, Michaud K, Wolfe F. Skin cancer, rheumatoid arthritis, and tumor necrosis factor inhibitors. J Rheumatol. 2005;32:2130-2135.
- Chambers CD, Johnson DL, Jones KL. Pregnancy outcome in women exposed to anti-TNF alpha medications: the OTIS rheumatoid arthritis in Pregnancy Study. Arthritis & Rheum 2004; 50: S479.
- Chambers CD. Safety of anti-TNF alpha medications in pregnancy. J Am Acad Dermatol 2005; 53 (Suppl 2) Ab8: 155-08.
- Cheifetz A, Smedley M, Martin S, Reiter M, Leone G, Mayer L et al. The incidence and management of infusion reactions to infliximab: a large center experience. Am J Gastroenterol 2003; 98(6):1315-24.
- Chung ES, Packer M, Lo KH, Fasanmade AA, Willerson JT. Randomized, double-blind, placebo-controlled, pilot trial of infliximab, a chimeric monoclonal antibody to tumor necrosis factor-alpha, in patients with moderate-to-severe heart failure: results of the anti-TNF Therapy Against Congestive Heart Failure (ATTACH) trial. Circulation 2003; 107(25):3133-40.
- Coates et al Rheumatology 2008;42:897
- Cohen S, Hurd E, Cush J, Schiff M, Weinblatt ME, Moreland LW et al. Treatment of rheumatoid arthritis with anakinra, a recombinant human interleukin-1 receptor antagonist, in combination with methotrexate: results of a twenty-four-week, multicenter, randomized, double-blind, placebo-controlled trial. Arthritis Rheum 2002; 46(3):614-24.
- Cohen SB, Moreland LW, Cush JJ, Greenwald MW, Block S, Shergy WJ et al. A multicentre, double blind, randomised, placebo controlled trial of anakinra (Kineret), a recombinant interleukin 1 receptor antagonist, in patients with rheumatoid arthritis treated with background methotrexate. Ann Rheum Dis 2004; 63(9):1062-8.
- Cohen SB, Emery P, Greenwald MW, Dougados M, Furie RA, Genovese MC et al. Rituximab for rheumatoid arthritis refractory to anti-tumor necrosis factor therapy: Results of a multicenter, randomized, double-blind, placebo-controlled, phase III trial evaluating primary efficacy and safety at twenty-four weeks. Arthritis Rheum 2006; 54(9):2793-806.
- Cole J, Busti A, Kazi S. The incidence of new onset congestive heart failure and heart failure exacerbation in Veteran's Affairs patients receiving tumor necrosis factor alpha antagonists. Rheumatol Int 2007; 27(4):369-73.
- Colombel JF, Loftus EV, Tremaine WJ, et al. Early postoperative complications are not increased in patients with Crohns disease treated perioperatively with infliximab or immunosuppressive therapy. Am J Gastroenterol 2004; 99: 878-83
- Colombel JF, D'Haens G, Rutgeerts P, Panes J. No new safety signals identified in Crohn's disease patients treated with infliximab in an interim review of the ENCORE registry. JCC. 2008;2.
- Colombel JF, Sandborn WJ, Panaccione R, Robinson AM, Lau W, Li J et al. Adalimumab safety in global clinical trials of patients with Crohn's disease. Inflamm Bowel Dis 2009; 15(9):1308-19.
- Corrao S, Pistone G, Arnone S, et al. Safety of etanercept therapy in rheumatoid patients undergoing surgery: preliminary report. Clin Rheumatol 2007; 26: 1513-5.
- Costenbader KH, Glass R, Cui J, Shadick N. Risk of serious infections and malignancies with anti-TNF antibody therapy in rheumatoid arthritis. JAMA. 2006;296:2201-4.
- Curtis JR, Kramer JM, Martin C, Saag KG, Patkar N, Shatin D et al. Heart failure among younger rheumatoid arthritis and Crohn's patients exposed to TNF-alpha antagonists. Rheumatology (Oxford) 2007; 46(11):1688-93.
- Cush JJ. Biological drug use: US perspectives on indications and monitoring. Ann Rheum Dis 2005; 64: iv18-iv23
- Dahlqvist SR, Engstrand S, Berglin E, Johnson O. Conversion towards an atherogenic lipid profile in rheumatoid arthritis patients during long-term infliximab therapy. Scand J Rheumatol 2006; 35(2):107-11.
- Danila MI, Patkar NM, Curtis JR, Saag KG, Teng GG. Biologics and heart failure in rheumatoid arthritis: are we any wiser? Curr Opin Rheumatol 2008; 20(3):327-33.
- Dechant C, Antoni C, Wendler et al. One year outcome of patients with severe psoriatic arthritis treated with infliximab. Arthritis & Rheum 2000; 43: S102.
- Den Broeder AA, Creemers MCW, Franssen J, et al. Risk factors for surgical site infections and other complications in elective surgery in patients with rheumatoid arthritis with special attention for antitumor necrosis factor: a large retrospective study. J Rheumatol 2007; 34: 689-95.
- D'Haens G. Risks and benefits of biologic therapy for inflammatory bowel diseases. Gut 2007; 56(5):725-32.
- Dixon et al AR 2006; 54: 2368
- Dixon et al AR 2007;56:2896
- Eaden JA, Abrams KR, Mayberry JF. The risk of colorectal cancer in ulcerative colitis: a meta-analysis. Gut. 2001;48:526-35.
- Edwards AG, Evans R, Dundon J, Haigh S, Hood K, Elwyn GJ.Personalised risk communication for informed decision making about taking screening tests. Cochrane Database Syst Rev. 2006 Oct 18;(4):CD001865.Update of: Cochrane Database Syst Rev. 2003;(1):CD001865.
- Edward J. Hollox, Ulrike Huffmeier, Patrick L.J.M. Zeeuwen, Raquel Palla, Jesús Lascorz, Diana Rodijk-Olthuis, Peter C.M. van de Kerkhof, Heiko Traupe, Gys de Jongh, Martin den Heijer, André Reis, John A.L. Armour, and Joost Schalkwijk . Psoriasis is associated with increased beta-defensin genomic copy number. Nat Genet. 2008 ; 40: 2325.)
- Ekbom A, Helmick C, Zack M, Adami HO. Increased risk of large-bowel cancer in Crohn's disease with colonic involvement. Lancet. 1990;336:357-59.
- Elkayam O, Caspi D, Reitblatt T, Charboneau D, Rubins JB. The effect of tumor necrosis factor blockade on the response to pneumococcal vaccination in patients with rheumatoid arthritis and ankylosing spondylitis. Semin Arthritis Rheum 2004; 33(4):283-8.
- Emery P, Fleischmann R, Filipowicz-Sosnowska A, Schechtman J, Szczepanski L, Kavanaugh A et al. The efficacy and safety of rituximab in patients with active rheumatoid arthritis despite methotrexate treatment: results of a phase IIB randomized, double-blind, placebo-controlled, dose-ranging trial. Arthritis Rheum 2006; 54(5):1390-400.
- Emery P, Keystone E, Tony HP, Cantagrel A, van Vollenhoven R, Sanchez A et al. IL-6 receptor inhibition with tocilizumab improves treatment outcomes in patients with rheumatoid arthritis refractory to anti-tumour necrosis factor biologicals: results from a 24-week multicentre randomised placebo-controlled trial. Ann Rheum Dis 2008; 67(11):1516-23.
- Falagas ME, Manta KG, Betsi GI, Pappas G. Infection-related morbidity and mortality in patients with connective tissue diseases: a systematic review. Clin Rheumatol 2007; 26(5):663-70.
- Farrell RJ, Alsahli M, Jeen YT, Falchuk KR, Peppercorn MA, Michetti P. Intravenous hydrocortisone premedication reduces antibodies to infliximab in Crohn's disease: a randomized controlled trial. Gastroenterology 2003; 124(4):917-24.
- FDA. Questions and Answers - TNF Blockers 8/25/2009. 2009. 13-11-2009.
- FDA. Information for Healthcare Professionals: Tumor Necrosis Factor (TNF) Blockers (marketed as Remicade, Enbrel, Humira, Cimzia, and Simponi). 2009. 13-11-2009.
- Ferrante et al, Inflamm Bowel Dis 2009;15:1062-70.
- Feyertag J, Dinhof G, Salzer H, Dunky A. Pregnancy in a rheumatoid arthritis patient treated with etanercept. Ann Rheum Dis 2004; 63 (Suppl 1): 198.
- Finck et al ARD 2009 May 15 Epub
- Fleischmann RM, Schechtman J, Bennett R, Handel ML, Burmester GR, Tesser J et al. Anakinra, a recombinant human interleukin-1 receptor antagonist (r-metHuIL-1ra), in patients with rheumatoid arthritis: A large, international, multicenter, placebo-controlled trial. Arthritis Rheum 2003; 48(4):927-34.
- Fleischmann RM, Tesser J, Schiff MH, Schechtman J, Burmester GR, Bennett R et al. Safety of extended treatment with anakinra in patients with rheumatoid arthritis. Ann Rheum Dis 2006; 65(8):1006-12.
- Fleischmann R, Baumgartner SW, Weisman MH, Liu T, White B, Peloso P. Long term safety of etanercept in elderly subjects with rheumatic diseases. Ann Rheum Dis. 2006;65:379-84.
- Fomin I, Caspi D, Levy V, Varsano N, Shalev Y, Paran D et al. Vaccination against influenza in rheumatoid arthritis: the effect of disease modifying drugs, including TNF alpha blockers. Ann Rheum Dis 2006; 65(2):191-4.
- Furst DE. The Risk of Infections with Biologic Therapies for Rheumatoid Arthritis. Semin Arthritis Rheum 2008.
- Furst DE, Keystone EC, Kirkham B, Kavanaugh A, Fleischmann R, Mease P et al. Updated consensus statement on biological agents for the treatment of rheumatic diseases, 2008. Ann Rheum Dis 2008; 67 Suppl 3:iii2-25.
- Garcia J, Joven B, Ruiz T et al. Pregnancy in women receiving antiTNF alpha therapy. Experience in Spain. Ann Rheum Dis 2006; 65 (Suppl 11): 317.
- Gelfand JM, Berlin J, Van VA, Margolis DJ. Lymphoma rates are low but increased in patients with psoriasis: results from a population-based cohort study in the United Kingdom. Arch Dermatol. 2003;139:1425-29.
- Gelfand JM, Shin DB, Neimann AL, Wang X, Margolis DJ, Troxel AB. The risk of lymphoma in patients with psoriasis. J Invest Dermatol. 2006;126:2194-201.
- Gelinck LB, Teng YK, Rimmelzwaan GF, van den Bemt BJ, Kroon FP, van Laar JM. Poor serological responses upon influenza vaccination in patients with rheumatoid arthritis treated with rituximab. Ann Rheum Dis 2007; 66(10):1402-3.
- Gelinck LB, van der Bijl AE, Beyer WE, Visser LG, Huizinga TW, van Hogezand RA et al. The effect of anti-tumour necrosis factor alpha treatment on the antibody response to influenza vaccination. Ann Rheum Dis 2008; 67(5):713-6.
- Genovese MC, Cohen S, Moreland L, Lium D, Robbins S, Newmark R et al. Combination therapy with etanercept and anakinra in the treatment of patients with rheumatoid arthritis who have been treated unsuccessfully with methotrexate. Arthritis Rheum 2004; 50(5):1412-9.
- Genovese MC, McKay JD, Nasonov EL, Mysler EF, da Silva NA, Alecock E et al. Interleukin-6 receptor inhibition with tocilizumab reduces disease activity in rheumatoid arthritis with inadequate response to disease-modifying antirheumatic drugs: the tocilizumab in combination with traditional disease-modifying antirheumatic drug therapy study. Arthritis Rheum 2008; 58(10):2968-80.
- Giles JT, Gelber AC, Nanda S, et al. TNF inhibitor therapy increases the risk of post operative orthopaedic infection in patients with rheumatoid arthritis [abstract]. Arthritis & Rheum 2004; 50 (suppl): S660.
- Golding A, Uzma JH, Giles JT. Rheumatoid arthritis and reproduction. Rheum Dis Clin N Am 2007; 33: 319-43.
- Gomez-Reino JJ, Carmona L, Angel Descalzo M. Risk of tuberculosis in patients treated with tumor necrosis factor antagonists due to incomplete prevention of reactivation of latent infection. Arthritis Rheum 2007; 57(5):756-61.
- Gottlieb AB, Gordon KB, Giannini EH. Malignancies from patients receiving etanercept across approved indications. Ann Rheum Dis. 2008;67 (Suppl II):322.
- Gottlieb A, Menter A, Mendelsohn A, Shen YK, Li S, Guzzo C et al. Ustekinumab, a human interleukin 12/23 monoclonal antibody, for psoriatic arthritis: randomised, double-blind, placebo-controlled, crossover trial. Lancet 2009; 373(9664):633-40.
- Haggerty HG, Abbott MA, Reilly TP, DeVona DA, Gleason CR, Tay L et al. Evaluation of immunogenicity of the T cell costimulation modulator abatacept in patients treated for rheumatoid arthritis. J Rheumatol 2007; 34(12):2365-73.
- Han PD, Cohen RD. Managing immunogenic responses to infliximab: treatment implications for patients with Crohn's disease. Drugs 2004; 64(16):1767-77.
- Hanauer SB, Wagner CL, Bala M, Mayer L, Travers S, Diamond RH et al. Incidence and importance of antibody responses to infliximab after maintenance or episodic treatment in Crohn's disease. Clin Gastroenterol Hepatol 2004; 2(7):542-53.
- Hannuksela-Svahn A, Pukkala E, Laara E, Poikolainen K, Karvonen J. Psoriasis, its treatment, and cancer in a cohort of Finnish patients. J Invest Dermatol. 2000;114:587-90.
- Hyrich KL, Symmons DPM, Watson KD, Silman AJ. Pregnancy outcome in women who were exposed to anti-tumour necrosis factor agents: results from a national population register. Arthritis & Rheum 2006; 54: 2701-2.
- Hyrich et al AR 2007; 56:13
- Iglesias E, OValle F, Salvatierra J, et al. Effect of blockade of tumor necrosis factor-a with etanercept on surgical wound healing in SWISS-OF1 mice. J Rheumatol 2009; doi 10.3899/jrheum.081285.
- Jansen PA, Rodijk-Olthuis D, Hollox EJ, Kamsteeg M, Tjabringa GS, de Jongh GJ, van Vlijmen-Willems IM, Bergboer JG, van Rossum MM, de Jong EM, den Heijer M, Evers AW, Bergers M, Armour JA, Zeeuwen PL, Schalkwijk J. Beta-defensin-2 protein is a serum biomarker for disease activity in psoriasis and reaches biologically relevant concentrations in lesional skin. PLoS One. 2009;4:e4725).
- Jess T, Loftus EV, Jr., Velayos FS, Harmsen WS, Zinsmeister AR, Smyrk TC et al. Risk of intestinal cancer in inflammatory bowel disease: a population-based study from olmsted county, Minnesota. Gastroenterology. 2006;130:1039-46.
- Joven BE, Garcia-Gonzales AJ, Ruiz T et al. Pregnancy in women receiving antiTNF therapy. Experience in Spain. Arthritis Rheum 2005; 52:S349.
- Kaine JL, Kivitz AJ, Birbara C, Luo AY. Immune responses following administration of influenza and pneumococcal vaccines to patients with rheumatoid arthritis receiving adalimumab. J Rheumatol 2007; 34(2):272-9.
- Kandiel A, Fraser AG, Korelitz BI, Brensinger C, Lewis JD. Increased risk of lymphoma among inflammatory bowel disease patients treated with azathioprine and 6-mercaptopurine. Gut. 2005;54:1121-25.
- Kaoskvik HS, Magnussen AM, Skomsvoll JF. One year follow-up of etanercept exposed pregnancies. Ann Rheum Dis 2005; 64: (Suppl III): 449.
- Kapetanovic MC, Larsson L, Truedsson L, Sturfelt G, Saxne T, Geborek P. Predictors of infusion reactions during infliximab treatment in patients with arthritis. Arthritis Res Ther 2006; 8(4):R131.
- Kapetanovic MC, Saxne T, Sjoholm A, Truedsson L, Jonsson G, Geborek P. Influence of methotrexate, TNF blockers and prednisolone on antibody responses to pneumococcal polysaccharide vaccine in patients with rheumatoid arthritis. Rheumatology (Oxford) 2006; 45(1):106-11.
- Kapetanovic MC, Saxne T, Nilsson JA, Geborek P. Influenza vaccination as model for testing immune modulation induced by anti-TNF and methotrexate therapy in rheumatoid arthritis patients. Rheumatology (Oxford) 2007; 46(4):608-11.
- Katz JA, Antoni CE, Keenan GF, et al. Outcome of pregnancy in women receiving infliximab for the treatment of Crohns disease and rheumatoid arthritis. Am J Gastroenterol 2004; 99: 2385-92.
- Kerekes G, Soltesz P, Der H, Veres K, Szabo Z, Vegvari A et al. Effects of rituximab treatment on endothelial dysfunction, carotid atherosclerosis, and lipid profile in rheumatoid arthritis. Clin Rheumatol 2009; 28(6):705-10.
- Kievit et al ARD 2009; 68: 844
- Kinder AJ, Edwards J, Samanta A, Nichol F. Pregnancy in a rheumatoid arthritis patient on infliximab and methotrexate. Rheumatology 2005; 43: 1196-7.
- Kiortsis DN, Mavridis AK, Filippatos TD, Vasakos S, Nikas SN, Drosos AA. Effects of infliximab treatment on lipoprotein profile in patients with rheumatoid arthritis and ankylosing spondylitis. J Rheumatol 2006; 33(5):921-3.
- Klink DT, Van Elburg RM, Schreurs MWJ, Van Well GTJ. Rituximab administration in third trimester of pregnancy suppresses neonatal B-cell development. Clin Development Immunol 2008; doi:10.1155/2008/271363.
- Kremer JM, Genant HK, Moreland LW, Russell AS, Emery P, Abud-Mendoza C et al. Effects of abatacept in patients with methotrexate-resistant active rheumatoid arthritis: a randomized trial. Ann Intern Med 2006; 144(12):865-76.
- Koren G, Inoue M. Do tumor necrosis factor inhibitors cause malformations in humans? J Rheumatol 2009; 36: 465-6.
- Kwon HJ, Cote TR, Cuffe MS, Kramer JM, Braun MM. Case reports of heart failure after therapy with a tumor necrosis factor antagonist. Ann Intern Med 2003; 138(10):807-11.
- Lamboglia F, DInca R, Olivia L, Bertomoro P, Sturniolo GC. Patient with severe Crohns disease became a father while on methotrexate and infliximab therapy. Inflamm Bowel Dis 2009; 15: 648-9.
- La Montagna G, Malesci D, Buono R, Valentini G. Asthenozoospermia in patients receiving anti-tumour necrosis factor a agents. Ann Rheum Dis 2005; 64: 1667.
- Langholz E, Munkholm P, Davidsen M, Binder V. Colorectal cancer risk and mortality in patients with ulcerative colitis. Gastroenterology. 1992;103:1444-51.
- Lequerre T, Vittecoq O, Klemmer N, Goeb V, Pouplin S, Menard JF et al. Management of infusion reactions to infliximab in patients with rheumatoid arthritis or spondyloarthritis: experience from an immunotherapy unit of rheumatology. J Rheumatol 2006; 33(7):1307-14.
- Leuven van SI, Hezemans R, Levels JH, Snoek S, Stokkers PC, Hovingh GK et al. Enhanced atherogenesis and altered high density lipoprotein in patients with Crohn's disease. J Lipid Res 2007; 48(12):2640-6.
- Lewis JD, Bilker WB, Brensinger C, Deren JJ, Vaughn DJ, Strom BL. Inflammatory bowel disease is not associated with an increased risk of lymphoma. Gastroenterology. 2001;121:1080-1087.
- Li LC, Adam P, Townsend AF, Stacey D, Lacaille D, Cox S, McGowan J, Tugwell P, Sinclair G, Ho K, Backman CL Improving healthcare consumer effectiveness: an Animated, Self-serve, Web-based Research Tool (ANSWER) for people with early rheumatoid arthritis.BMC Med Inform Decis Mak. 2009 Aug 20; 9: 40.
- Lichtenstein GR, Feagan BG, Cohen RD, Salzberg BA, Diamond RH, Chen DM et al. Serious infections and mortality in association with therapies for Crohn's disease: TREAT registry. Clin Gastroenterol Hepatol 2006; 4(5):621-30.
- Lichtenstein G, Cohen R, Feagan B. Safety of Infliximab and Other Crohn's Disease Therapies: TreatTM
- Registry Data with 24,575 Patient-Years of Follow-up. Am J Gastr. 2008;S436.
- Lockshin MD. Treating rheumatic diseases in pregnancy: dos and donts. Ann Rheum Dis 2006; 65 (Supll III) iii58-60.
- Listing J, Strangfeld A, Kekow J, Schneider M, Kapelle A, Wassenberg S et al. Does tumor necrosis factor alpha inhibition promote or prevent heart failure in patients with rheumatoid arthritis? Arthritis Rheum 2008; 58(3):667-77.
- Loftus EV, Jr., Tremaine WJ, Habermann TM, Harmsen WS, Zinsmeister AR, Sandborn WJ. Risk of lymphoma in inflammatory bowel disease. Am J Gastroenterol. 2000;95:2308-12.
- Long MD, Herfarth HH, Pipkin C, Porter CQ, Sandler RS, Kappelman M. Increased Risk for Non-Melanoma Skin Cancer in Patients with Inflammatory Bowel Disease. Clin Gastroenterol Hepatol. 2009.
- Mackey AC, Green L, Liang LC, Dinndorf P, Avigan M. Hepatosplenic T cell lymphoma associated with infliximab use in young patients treated for inflammatory bowel disease. J Pediatr Gastroenterol Nutr. 2007;44:265-67.
- Mackey AC, Green L, Leptak C, Avigan M. Hepatosplenic T cell lymphoma associated with infliximab use in young patients treated for inflammatory bowel disease: update. J Pediatr Gastroenterol Nutr. 2009;48:386-88.
- Mahadevan U, Kane S, Sandborn WJ et al. Intentional infliximab use during pregnancy for induction or maintenance of remission in Crohns disease. Aliment Pharmacol Ther 2005; 21: 733-8.
- Mahadevan U, Terdiman JP, Aron J, et al. Infliximab and semen quality in men with inflammatory bowel disease. Inflamm Bowel Dis 2005; 11: 395-9.
- Maini RN, Breedveld FC, Kalden JR, Smolen JS, Davis D, Macfarlane JD et al. Therapeutic efficacy of multiple intravenous infusions of anti-tumor necrosis factor alpha monoclonal antibody combined with low-dose weekly methotrexate in rheumatoid arthritis. Arthritis Rheum 1998; 41(9):1552-63.
- Maish GO 3rd, Shumate ML, Ehrlich HP, et al. Interleukin-1 receptor antagonist attenuates tumor necrosis factor-induced alterations in wound breaking strength. J Trauma 1999; 47 (3): 533-4.
- Mann DL, McMurray JJ, Packer M, Swedberg K, Borer JS, Colucci WS et al. Targeted anticytokine therapy in patients with chronic heart failure: results of the Randomized Etanercept Worldwide Evaluation (RENEWAL). Circulation 2004; 109(13):1594-602.
- Marcil I, Stern RS. Squamous-cell cancer of the skin in patients given PUVA and ciclosporin: nested cohort crossover study. Lancet. 2001;358:1042-45.
- McCharty AE, Mileno D. Prevention and treatment of travel-related infections in compromised hosts Curr Opin Infect Dis 2006;19:450-55
- Mc Keever KR, Beyer J, Ortega S, et al. An embryo-fetal development study in cynomolgus monkeys with rituximab, an anti-CD20 antibody. Toxicol Sci 2003; 72 (Suppl): 172 (abstract).
- Mease PJ, Ritchlin CT, Martin RW, Gottlieb AB, Baumgartner SW, Burge DJ et al. Pneumococcal vaccine response in psoriatic arthritis patients during treatment with etanercept. J Rheumatol 2004; 31(7):1356-61.
- Mehta NN, Azfar RS, Shin DB, Neimann AL, Troxel AB, Gelfand JM. Patients with severe psoriasis are at increased risk of cardiovascular mortality: cohort study using the General Practice Research Database. Eur Heart J 2009.
- Melmed GY, Ippoliti AF, Papadakis KA, Tran TT, Birt JL, Lee SK et al. Patients with inflammatory bowel disease are at risk for vaccine-preventable illnesses. Am J Gastroenterol 2006; 101(8):1834-40.
- Moreland LW, Weinblatt ME, Keystone EC, Kremer JM, Martin RW, Schiff MH et al. Etanercept treatment in adults with established rheumatoid arthritis: 7 years of clinical experience. J Rheumatol. 2006;33:854-61.
- Murashima A, Watanabe N, Ozawa N, Saito H, Yamaguchi K. Etanercept during pregnancy and lactation in a patient with rheumatoid arthritis: drug levels in maternal serum, cord blood, breast milk and the infants serum. Ann Rheum Dis 2009; 68: 1793.
- Nannini C, Cantini F, Niccoli L, Cassara E, Salvarani C, Olivieri I et al. Single-center series and systematic review of randomized controlled trials of malignancies in patients with rheumatoid arthritis, psoriatic arthritis, and ankylosing spondylitis receiving anti-tumor necrosis factor alpha therapy: is there a need for more comprehensive screening procedures? Arthritis Rheum. 2009;61:801-12.
- Neven N, Vis M, Voskuyl AE, et al. Adverse events in patients with rheumatoid arthritis treated with infliximab in daily clinical practice. Ann Rheum Dis 2005; 64: 645-6.
- Nurmohamed MT. Atherogenic lipid profiles and its management in patients with rheumatoid arthritis. Vasc Health Risk Manag 2007; 3(6):845-52.
- O'Connor AM, Stacey D, Rovner D, Holmes-Rovner M, Tetroe J, Llewellyn-Thomas H, Entwistle V, Rostom A, Fiset V, Barry M, Jones J.Decision aids for people facing health treatment or screening decisions. Cochrane Database Syst Rev. 2001;(3):Update in: CD001431Cochrane Database Syst Rev. 2003;(2):CD001431.
- ODonnell S, OMorain C. Use of antitumour necrosis factor therapy in inflammatory bowel disease during pregnancy and conception. Aliment Pharmacol Ther 2008; 27: 885-94.
- Ojeda-Uribe M, Gilliot C, Jung G, et al. Administration of rituximab during the first trimester of pregnancy without consequences for the newborn. J Perenatol 2006; 26: 252-5.
- Okada SK, Siegel JN. Risk of serious infections and malignancies with anti-TNF antibody therapy in rheumatoid arthritis. JAMA. 2006;296:2201-2.
- Oren S, Mandelboim M, Braun-Moscovici Y, Paran D, Ablin J, Litinsky I et al. Vaccination against influenza in patients with rheumatoid arthritis: the effect of rituximab on the humoral response. Ann Rheum Dis 2008; 67(7):937-41.
- Ostensen M, Obrist-Eigenmann G. Etanercept in breast milk. J Rheumatol 2004; 31: 1017-8.
- Ostensen M, Lockshin M, Doria A, et al. Update on safety during pregnancy of biological agents and some immunosuppressive antirheumatic drugs. Rheumatology 2008; 47: iii28-31.
- Ostensen M, Förger F. Management of RA medications in pregnant patients. Nat Rev Rheumatol 2009; 5: 382-90.
- Papa A, Danese S, Urgesi R, Grillo A, Guglielmo S, Roberto I et al. Early atherosclerosis in patients with inflammatory bowel disease. Eur Rev Med Pharmacol Sci 2006; 10(1):7-11.
- Pappas DA, Giles JT. Do antitumor necrosis factor agents increase the risk of postoperative orthopedic infections? Curr Opin Rheumatol 2008; 20(4):450-6.
- Pathirana D, Hillemanns P, Petry KU, Becker N, Brockmeyer NH, Erdmann R et al. Short version of the German evidence-based Guidelines for prophylactic vaccination against HPV-associated neoplasia. Vaccine 2009; 27(34):4551-9.
- Palascak-Juif V, Bouvier AM, Cosnes J, Flourie B, Bouche O, Cadiot G et al. Small bowel adenocarcinoma in patients with Crohn's disease compared with small bowel adenocarcinoma de novo. Inflamm Bowel Dis. 2005;11:828-32.
- Paschou S, Voulgari PV, Vrabile IG, Saougou IG, Drosos AA. Fertility and reproduction in male patients with ankylosing spondylitis treated with infliximab. J Rheumatol 2009; 36: 351-4.
- Paul CF, Ho VC, McGeown C, Christophers E, Schmidtmann B, Guillaume JC et al. Risk of malignancies in psoriasis patients treated with cyclosporine: a 5 y cohort study. J Invest Dermatol. 2003;120:211-16.
- Peters MJ, Vis M, van Halm VP, Wolbink GJ, Voskuyl AE, Lems WF et al. Changes in lipid profile during infliximab and corticosteroid treatment in rheumatoid arthritis. Ann Rheum Dis 2007; 66(7):958-61.
- Peltier M, James D, Ford J et al. Infliximab levels in breast-milk of a nursing Crohns patient. Presented at the Am Coll of Gastroenterol 66th Ann Scient Meeting 2001; Las Vegas (NV), Oct 22-26, 2001
- Peyrin-Biroulet L, Deltenre P, de Suray N, Branche J, Sandborn WJ, Colombel JF. Efficacy and safety of tumor necrosis factor antagonists in Crohn's disease: meta-analysis of placebo-controlled trials. Clin Gastroenterol Hepatol 2008; 6(6):644-53.
- Pham T, Claudepierre P, Deprez X, Fautrel B, Goupille P, Hilliquin P, Masson C, Morel J, Puéchal X, Saraux A, Schaeverbeke T, Mariette X, Sibilia. Anti-TNF alpha therapy and safety monitoring. Clinical tool guide elaborated by the Club Rhumatismes et Inflammations (CRI), section of the French Society of Rheumatology (Société Française de Rhumatologie, SFR). Joint Bone Spine. 2005 Jun;72 Suppl 1:S1-58.
- Pham T, Fautrel B, Gottenberg JE, Goupille P, Hachulla E, Masson C, Morel J, Mouthon L, Saraux A, Schaeverbeke T, Wendling D, Mariette X, Sibilia; Rheumatic Diseases & Inflammation Group (Club Rhumatismes et Inflammation, CRI) of the French Society for Rheumatology (Société Française de Rhumatologie, SFR). Rituximab (MabThera) therapy and safety management. Clinical tool guide. Joint Bone Spine. 2008 Jun;75 Suppl 1:S1-99.
- Pham T, Claudepierre P, Constantin A, Fautrel B, Gossec L, Gottenberg JE, Goupille P, Hachulla E, Masson C, Morel J, Saraux A, Schaeverbeke T, Wendling D, Mariette X, Sibilia J. Abatacept therapy and safety management Joint Bone Spine. 2009 May;76 Suppl 1:S3-S55
- Pichler WJ. Adverse side-effects to biological agents. Allergy 2006; 61(8):912-20.
- Pieringer H, Stuby U, Biesenbach G. Patients with rheumatoid arthritis undergoing surgery: how should we deal with antirheumatic treatment? Semin Arthritis Rheum 2007; 36: 278-86.
- Pijpe J, van Imhoff GW, Spijkervet FK, Roodenburg JL, Wolbink GJ, Mansour K et al. Rituximab treatment in patients with primary Sjogren's syndrome: an open-label phase II study. Arthritis Rheum 2005; 52(9):2740-50.
- Pocock et al Rheumatology 2008; 47:1073
- Popa C, van Tits LJ, Barrera P, Lemmers HL, van den Hoogen FH, van Riel PL et al. Anti-inflammatory therapy with tumour necrosis factor alpha inhibitors improves high-density lipoprotein cholesterol antioxidative capacity in rheumatoid arthritis patients. Ann Rheum Dis 2009; 68(6):868-72.
- Pradeep et al Rheumatology 2008; 47: 1726
- Radstake TR, Svenson M, Eijsbouts AM, van den Hoogen FH, Enevold C, van Riel PL et al. Formation of antibodies against infliximab and adalimumab strongly correlates with functional drug levels and clinical responses in rheumatoid arthritis. Ann Rheum Dis 2008.
- Richtlijn diagnostiek en behandeling van inflammatoire darmziekten bij volwassenen. 2008. CBO
- Richtlijn voor de diagnostiek en behandeling van Ankyloserende Spondylitis. 2009.
- Rohekar S, Tom BD, Hassa A, Schentag CT, Farewell VT, Gladman DD. Prevalence of malignancy in psoriatic arthritis. Arthritis Rheum. 2008;58:82-87.
- Rosner I, Haddad A, Boulman N, et al. Pregnancy in rheumatology patients exposed to anti-tumour necrosis factor therapy. Rheumatology 2007 (letter); 46: 1508
- Roux CH, Brocq O, Breuil V, Albert C, Euller-Ziegler L. Pregnancy in rheumatology patients exposed to anti-tumour necrosis factor therapy. Rheumatology 2007; 46: 695-8.
- Rump JA, Usadel S, Schônborn H. Pregnancy and etanercept. Two cases and follow-up. Ann Rheum Dis 2004; 63 (Suppl 1): 182.
- Rutter MD, Saunders BP, Wilkinson KH, Rumbles S, Schofield G, Kamm MA et al. Thirty-year analysis of a colonoscopic surveillance program for neoplasia in ulcerative colitis. Gastroenterology. 2006;130:1030-1038.
- Ruyssen-Witrand A, Gossec L, Salliot C, et al. Surgical procedures have a high complication rate in rheumatic patients reveiving TNF alpha blockers: a systematic retrospective study of 770 patients. Arthritis & Rheum 2005; 52 (suppl): S339.
- Saag KG, Teng GG, Patkar NM, Anuntiyo J, Finney C, Curtis JR et al. American College of Rheumatology 2008 recommendations for the use of nonbiologic and biologic disease-modifying antirheumatic drugs in rheumatoid arthritis. Arthritis Rheum of Arthritis Care & Res 2008; 59(6):762-84.
- Saini R, Shupack JL. Psoriasis: to cut or not to cut, what say you? Dermatol Surg. 2003 Jul;29(7):735-40).
- Salliot C, Dougados M, Gossec L. Risk of serious infections during rituximab, abatacept and anakinra treatments for rheumatoid arthritis: meta-analyses of randomised placebo-controlled trials. Ann Rheum Dis 2009; 68(1):25-32.
- Salmon JE, Alpert D. Are we coming to terms with tunor necrosis factor inhibition in pregnancy? Arthritis & Rheum 2006; 54: 2353-5.
- Schiff MH, Burmester GR, Kent JD, Pangan AL, Kupper H, Fitzpatrick SB et al. Safety analyses of adalimumab (HUMIRA) in global clinical trials and US postmarketing surveillance of patients with rheumatoid arthritis. Ann Rheum Dis. 2006;65:889-94.
- Seriolo B, Paolino S, Sulli A, Fasciolo D, Cutolo M. Effects of anti-TNF-alpha treatment on lipid profile in patients with active rheumatoid arthritis. Ann N Y Acad Sci 2006; 1069:414-9.
- Setoguchi S, Solomon DH, Weinblatt ME, Katz JN, Avorn J, Glynn RJ et al. Tumor necrosis factor alpha antagonist use and cancer in patients with rheumatoid arthritis. Arthritis Rheum. 2006;54:2757-64.
- Setoguchi S, Schneeweiss S, Avorn J, Katz JN, Weinblatt ME, Levin R et al. Tumor necrosis factor-alpha antagonist use and heart failure in elderly patients with rheumatoid arthritis. Am Heart J 2008; 156(2):336-41.
- Shale MJ. The implications of anti-tumour necrosis factor therapy for viral infection in patients with inflammatory bowel disease. Br Med Bull 2009.
- Shao LM, Chen MY, Cai JT. Meta-analysis: the efficacy and safety of certolizumab pegol in Crohn's disease. Aliment Pharmacol Ther 2009; 29(6):605-14.
- Sibilia J, Westhovens R. Safety of T-cell co-stimulation modulation with abatacept in patients with rheumatoid arthritis. Clin Exp Rheumatol. 2007;25:S46-S56.
- Siegel CA, Marden SM, Persing SM, Larson RJ, Sands BE. Risk of Lymphoma Associated With Combination Anti-Tumor Necrosis Factor and Immunomodulator Therapy for the Treatment of Crohn's Disease: A Meta-Analysis 94 94. Clin Gastroenterol Hepatol. 2009;7:874-81.
- Sills ES. Perloc M, Tucker MJ, Kaplan CD, Palermo GD. Successful ovulation induction, conception, and normal delivery after chronic therapy with etanercept: a recombinant fusion anti-cytokine treatment for rheumatoid arthritis. Am J Repord Immunol 2001; 46: 366-8.
- Simister NE. Placental transport of immunoglobulins. Vaccine 2003; 21: 3365-9.
- Simon TA, Smitten AL, Franklin J, Askling J, Lacaille D, Wolfe F et al. Malignancies in the rheumatoid arthritis abatacept clinical development programme: an epidemiological assessment. Ann Rheum Dis. 2009;68:1819-26.
- Smitten AL, Simon TA, Hochberg MC, Suissa S. A meta-analysis of the incidence of malignancy in adult patients with rheumatoid arthritis. Arthritis Res Ther. 2008;10:R45.
- Spanakis E, Sidiropoulos P, Papadakis J, Ganotakis E, Katsikas G, Karvounaris S et al. Modest but sustained increase of serum high density lipoprotein cholesterol levels in patients with inflammatory arthritides treated with infliximab. J Rheumatol 2006; 33(12):2440-6.
- Stockdale J, Goodacre L. 'It's magic stuff': the experiences of patients with ankylosing spondylitis taking anti-TNF-alpha medication. Musculoskeletal Care. 2009 Sep;7(3):162-77.
- Strangfeld A, Listing J, Herzer P, Liebhaber A, Rockwitz K, Richter C et al. Risk of herpes zoster in patients with rheumatoid arthritis treated with anti-TNF-alpha agents. JAMA 2009; 301(7):737-44.
- Talwalker SC, Grennan DM, Gray J, et al. Tumour necrosis factor a antagonists and early postoperative complications in patients with inflammatory joint disease undergoing elective orthopaedic surgery. Ann Rheum Dis 2005; 64: 650-1.
- Thurlings RM, Teng O, Vos K, Gerlag DM, Aarden L, Stapel SO et al. Clinical response, pharmacokinetics, development of human anti-chimeric antibodies, and synovial tissue response to rituximab treatment in patients with rheumatoid arthritis. Ann Rheum Dis 2009.
- Topstad DR, Panaccione R, Heine JA, et al. Combined seton placement , infliximab infusion and maintenance immunosuppressives improve healing rate in fistulizing anorectal Crohns disease. Dis Colon Rectum 2003; 46: 577-83
- Toruner M, Loftus EV, Jr., Harmsen WS, Zinsmeister AR, Orenstein R, Sandborn WJ et al. Risk factors for opportunistic infections in patients with inflammatory bowel disease. Gastroenterology 2008; 134(4):929-36.
- Tsuru T, Suzaki M, Yoshio N, Mima T, Nakashima H, Amamoto T et al. Immune response to influenza vaccine in patients during the treatment with tocilizumab-comparison with conventional DMARDs and TNF inhibitors. Ann Rheum Dis 2008;67(Supp lI):339 . 2009.
- Tuberculosis associated with blocking agents against tumor necrosis factor-alpha--California, 2002-2003. MMWR Morb Mortal Wkly Rep 2004; 53(30):683-6.
- Vasilauskas EA, Church JA, Silverman N, et al. Case report: evidence for trans-placental transfer of maternally administered infliximab to the newborn. Clin Gastroenterol Hepatol 2006; 4: 1255-8.
- Vermeire S, Noman M, Van Assche G, Baert F, D'Haens G, Rutgeerts P. Effectiveness of concomitant immunosuppressive therapy in suppressing the formation of antibodies to infliximab in Crohn's disease. Gut 2007; 56(9):1226-31.
- Vis M, Nurmohamed MT, Wolbink G, Voskuyl AE, de Koning M, Van de Stadt R et al. Short term effects of infliximab on the lipid profile in patients with rheumatoid arthritis. J Rheumatol 2005; 32(2):252-5.
- Visvanathan S, Keenan GF, Baker DG, Levinson AI, Wagner CL. Response to pneumococcal vaccine in patients with early rheumatoid arthritis receiving infliximab plus methotrexate or methotrexate alone. J Rheumatol 2007; 34(5):952-7.
- Vries de MK, Wolbink GJ, Stapel SO, de Vrieze H, van Denderen JC, Dijkmans BA et al. Decreased clinical response to infliximab in ankylosing spondylitis is correlated with anti-infliximab formation. Ann Rheum Dis 2007; 66(9):1252-4.
- Vries de MK, Wolbink GJ, Stapel SO, de Groot ER, Dijkmans BA, Aarden LA et al. Inefficacy of infliximab in ankylosing spondylitis is correlated with antibody formation. Ann Rheum Dis 2007; 66(1):133-4.
- Weinblatt M, Combe B, Covucci A, Aranda R, Becker JC, Keystone E. Safety of the selective costimulation modulator abatacept in rheumatoid arthritis patients receiving background biologic and nonbiologic disease-modifying antirheumatic drugs: A one-year randomized, placebo-controlled study. Arthritis Rheum 2006; 54(9):2807-16.
- Weinblatt M, Schiff M, Goldman A, Kremer J, Luggen M, Li T et al. Selective costimulation modulation using abatacept in patients with active rheumatoid arthritis while receiving etanercept: a randomised clinical trial. Ann Rheum Dis 2007; 66(2):228-34.
- Wendling D, Balblanc J-C, Brousse A, et al. Surgery in patients receiving anti-tumour necrosis factor alpha treatment in rheumatoid arthritis: an observational study on 50 surgical procedures. Ann Rheum Dis 2005; 64: 1378-9.
- West RL, Zelinkova Z, Wolbink GJ, Kuipers EJ, Stokkers PC, van der Woude CJ. Immunogenicity negatively influences the outcome of adalimumab treatment in Crohn's disease. Aliment Pharmacol Ther 2008; 28(9):1122-6.
- William G. Dixon, Kath D. Watson, Mark Lunt, BSRBR Control Centre Consortium, Kimme L. Hyrich, Deborah PM Symmons The Influence of Anti-TNF Therapy upon Cancer Incidence in Patients with Rheumatoid Arthritis (RA) who have had Prior Malignancy: Results from the BSRBR. ARD 2008; Suppl
- Wolbink GJ, Vis M, Lems W, Voskuyl AE, de Groot E, Nurmohamed MT et al. Development of antiinfliximab antibodies and relationship to clinical response in patients with rheumatoid arthritis. Arthritis Rheum 2006; 54(3):711-5.
- Wolfe F, Michaud K. Heart failure in rheumatoid arthritis: rates, predictors, and the effect of anti-tumor necrosis factor therapy. Am J Med 2004; 116(5):305-11.
- Wolfe F, Michaud K. The effect of methotrexate and anti-tumor necrosis factor therapy on the risk of lymphoma in rheumatoid arthritis in 19,562 patients during 89,710 person-years of observation. Arthritis Rheum. 2007;56:1433-39.
- Yokota S, Imagawa T, Mori M, Miyamae T, Aihara Y, Takei S et al. Efficacy and safety of tocilizumab in patients with systemic-onset juvenile idiopathic arthritis: a randomised, double-blind, placebo-controlled, withdrawal phase III trial. Lancet 2008; 371(9617):998-1006.
- Zink A, Askling J, Dixon WG, Klareskog L, Silman AJ, Symmons DP. European biologicals registers: methodology, selected results and perspectives. Ann Rheum Dis. 2009;68:1240-1246.
Verantwoording
Autorisatiedatum en geldigheid
Laatst beoordeeld : 01-01-2011
Laatst geautoriseerd : 01-01-2011
Geplande herbeoordeling : 01-01-2014
De Nederlandse Vereniging voor Reumatologie is als houder van deze richtlijn de eerstverantwoordelijke voor de actualiteit van deze richtlijn. Uiterlijk in 2013 bepaalt de NVR of deze richtlijn nog actueel is. Zo nodig wordt een nieuwe werkgroep geïnstalleerd om de richtlijn te herzien. De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De andere aan deze richtlijn deelnemende beroepsverenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid ten aanzien van het bewaken van de actualiteit van de aanbevelingen in de richtlijn. Hen wordt verzocht relevante ontwikkelingen binnen hun vakgebied kenbaar te maken aan de eerstverantwoordelijke.
Algemene gegevens
Met ondersteuning van de afdeling Ondersteuning Professionele Kwaliteit van de Orde van Medisch Specialisten. De richtlijnontwikkeling werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (= SKMS).
Doel en doelgroep
Deze richtlijn geeft een leidraad voor de dagelijkse praktijk van het gebruik van Biologicals. De richtlijn heeft een algemeen karakter, kan gebruikt worden om beroepsspecifieke richtlijnen te formuleren en biedt aanknopingspunten voor bijvoorbeeld lokale (instituuts- of regiogebonden) protocollen en/of zorgafspraken.
De richtlijn is primair geschreven voor medisch specialisten die patiënten met chronische ontstekingsziekten (IMID = Immune Mediated Inflammatory Disorders) behandelen met biologicals, alsmede voor deze patiënten zelf en hun overige behandelaars.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2009 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die met biologicals te maken hebben.
Bij het samenstellen van de werkgroep is rekening gehouden met geografische spreiding en evenredige vertegenwoordiging van verschillende verenigingen, ‘scholen’ en academische achtergrond. De werkgroepleden zijn door de wetenschappelijke verenigingen gemandateerd voor deelname en de samenstelling van de werkgroep is goedgekeurd door alle deelnemende wetenschappelijke verenigingen. De werkgroepleden zijn gezamenlijk verantwoordelijk voor de tekst.
- Dr. D.L. Baeten, reumatoloog, Academisch Medisch Centrum, Amsterdam
- Dr. M. Bijl, reumatoloog, Universitair Medisch Centrum Groningen
- Prof. dr. J.W.J. Bijlsma, reumatoloog, Universitair Medisch Centrum Utrecht (voorzitter)
- Dr. A.A. van Bodegraven, maag-, darm-, leverarts, VU Medisch Centrum, Amsterdam
- Dr. P.L.A. van Daele, internist-klinisch immunoloog, Erasmus Medisch Centrum, Rotterdam
- Prof. dr. M. Drent, longarts, Academisch Ziekenhuis Maastricht
- Mevr. drs. G.J. Geven, Reumapatiëntenbond, Amersfoort
- Mevr. drs. J.W. Hagemeijer, senior adviseur, Orde van medisch Specialisten, Utrecht
- Dr. T.L.Th.A. Jansen, reumatoloog, Medisch Centrum Leeuwarden
- Prof. dr. M.A.F.J. van de Laar, reumatoloog, Medisch Spectrum Twente, Enschede
- Prof. dr. R.B.M. Landewé, reumatoloog, Academisch Ziekenhuis Maastricht
- Prof. dr. W.F. Lems, reumatoloog, VU medisch centrum, Amsterdam
- Dr. M.T. Nurmohamed, reumatoloog, Jan van Breemen Instituut, Amsterdam
- Dr. E. Prens, dermatoloog, Erasmus Medisch Centrum, Rotterdam
- Mevr. drs. M.M.J.H. Scholte-Voshaar, Reumapatiëntenbond, Amersfoort
- Mevr. drs. M. Wessels, informatiespecialist, Orde van Medisch Specialisten, Utrecht
Belangenverklaringen
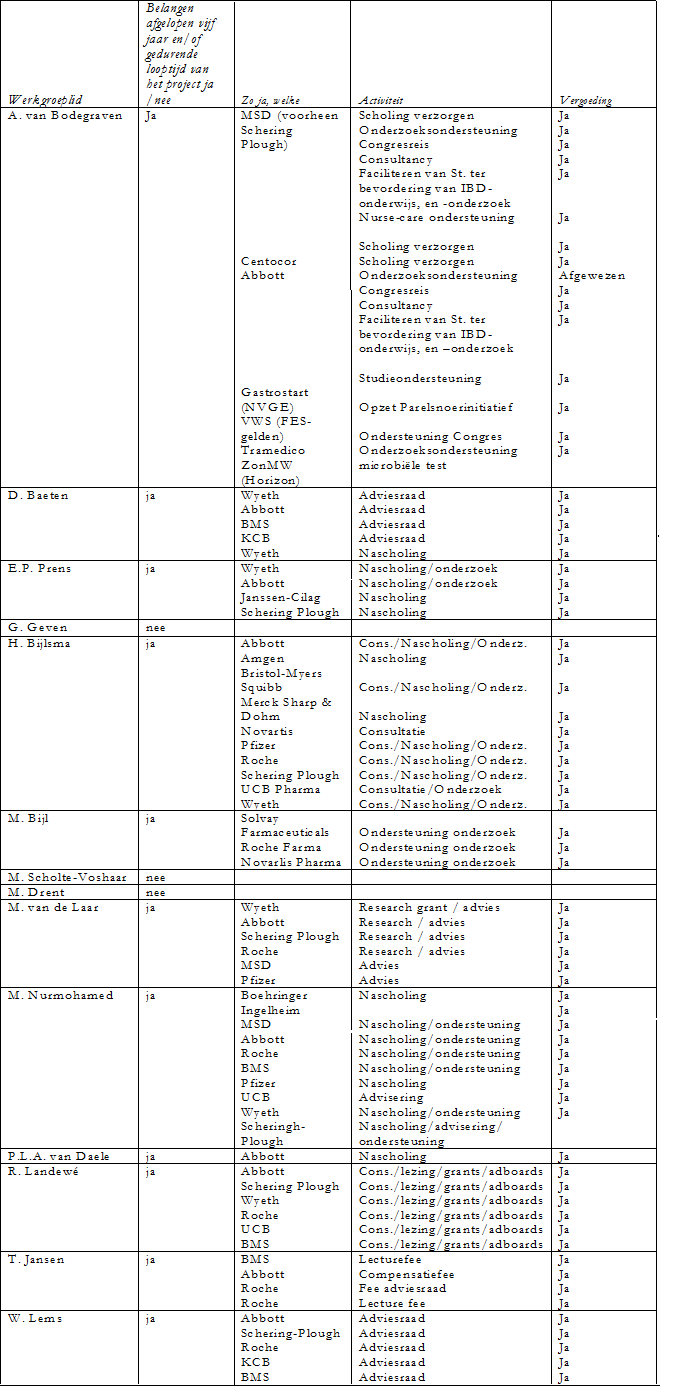
De werkgroepleden is gevraagd om aan te geven of er sprake is van een mogelijke belangenverstrengeling met commerciële bedrijven. Een overzicht hiervan is hieronder weergegeven. De verklaringen van werkgroepleden over mogelijke financiële belangenverstrengeling ligt ter inzage bij de afdeling Ondersteuning Professionele Kwaliteit van de Orde van Medisch Specialisten. Uit de ingevulde belangenverklaringen blijkt dat de werkgroepleden banden met de farmaceutische industrie hebben en dat deze banden gezien het onderwerp belangrijk zijn. Er wordt geconcludeerd dat deze banden geen invloed hebben gehad bij het totstandkomen van de richtlijn.
Inbreng patiëntenperspectief
Gedurende de ontwikkeling van de richtlijn is nadrukkelijk aandacht besteed aan het in kaart brengen van het patiëntenperspectief. In de werkgroep hebben twee patiëntenvertegenwoordigers zitting genomen en zij brachten het perspectief van de patiënten naar voren tijdens de bespreking van de teksten en de formulering van de aanbevelingen. Daarnaast is halverwege het traject een focusgroep georganiseerd waaraan 9 patiënten hebben deelgenomen. De uitgangsvragen zijn voorgelegd aan de leden van de focusgroep en hen is gevraagd naar hun ervaringen en overwegingen die zij van belang achten bij het formuleren van de aanbevelingen. Hiervan is een verslag gemaakt en aan de leden voorgelegd ter verifiëring en eventuele aanvulling. De leden van het schrijverscollectief hebben gebruikgemaakt van de inhoud van deze documentatie voor de formulering van overwegingen vanuit patiëntenperspectief. Een verslag hiervan is hieronder te vinden.
Patiëntenperspectief – verslag focusgroep
In totaal hebben 9 patiënten hun medewerking verleend aan het in kaart brengen van het patiëntenperspectief. Twee mannelijke patiënten met Sarcoidose met Remicade (via infuuskliniek (1 X p.m.) of Humira zelf injecteren (1X p.w.), één mannelijke patiënt met Psoriasis Enbrel zelf injecteren (1X p.w.), twee vrouwen met RA (Enbrel en Rituximab), één mannelijke patiënt met RA (Enbrel), twee vrouwelijke patiënten met Ziekte van Crohn (Humira en Remicade).
Drie personen waren aanwezig bij de focusgroepbijeenkomst die gehouden is op 12 november 2009. De overige 5 personen waren niet in staat om aanwezig te zijn en hebben op digitale wijze hun input geleverd door per uitgangsvraag hun ervaringen terug te koppelen.
Naast het bespreken van de ervaringen is ook gevraagd naar overwegingen die vanuit het perspectief van de patiënt van belang zijn en die naar hun idee meegewogen dienen te worden bij de formulering van de aanbevelingen.
Uit de besprekingen is naar voren gekomen dat de patiënten de geformuleerde uitgangsvragen complex vinden. De patiënten hebben aangegeven dat het maken van een patiëntenversie van de richtlijn belangrijk is omdat nog veel onduidelijk is over het gebruik van biologicals. Door het ontwikkelen van een patiëntenversie van de richtlijn ontvangen de patiënten een instrument waarmee zij ook kunnen bijdragen aan het goed en verantwoord gebruik van biologicals. Hierbij is als voorwaarde gesteld dat de patiëntenversie toegankelijk geschreven moet worden.
Alle deelnemers waren lid van een patiëntenvereniging en ervaren dit als zeer plezierig. Het geeft onder meer de mogelijkheid tot het uitwisselen van informatie met lotgenoten.
VOORAFGAANDE AAN DE BEHANDELING MET BIOLOGICALS: |
Overweging vanuit het patiëntenperspectief bij UV 1: - Patiënten geven aan dat de aanloop naar de behandeling met biologicals overwegend een langdurig proces is geweest. Er wordt overgegaan tot biologicals als alle andere behandelingsvormen niet blijken te helpen of te veel bijwerkingen veroorzaken. - Patiënten vinden het belangrijk dat alle aspecten die van belang zijn bij de behandeling van biologicals worden onderzocht, maar hebben geen zicht op welke aspecten dit dan moeten zijn. Zij geven aan dat het echter belangrijk is dat zij door de specialist of door de verpleegkundige deelgenoot worden gemaakt van het afwegingsproces door informatie te ontvangen zodat zij zelf actief kunnen meewerken aan het zorgproces. |
Overweging vanuit het patiëntenperspectief bij UV 2: - Patiënten vinden het belangrijk dat de arts door wie zij worden behandeld deskundig is, zodat zij erop kunnen vertrouwen in goede handen te zijn. - De (voorschrijvende) medisch specialist dient de regie in handen te houden en daarbij is het overleg met de andere betrokken professionals belangrijk. - Het is belangrijk dat de professionals communicatief zijn en duidelijk uitleg kunnen geven op niveau van de leek. Daarnaast is het wenselijk dat de medisch specialist toegankelijk en laagdrempelig is bij vragen; te weten via de telefoon of email. - Als het niet goed gaat met de patiёnt is het belangrijk dat de medisch specialist confronterend en direct is door aan te geven dat het helemaal niet goed gaat, dat de patiënt zich overvraagt of dat bijvoorbeeld gestopt moet worden met werken. Het is daarbij belangrijk dat de patiënt geen ruimte wordt gegeven om te marchanderen. - De partner is samen met de patiënt ziek en hiermee een essentiёle schakel die duidelijk betrokken behoort te worden in het zorgproces. |
BIJWERKINGEN VAN BIOLOGICALS: |
Overweging vanuit het patiëntenperspectief bij UV 3: - Patiënten vinden het belangrijk dat zij duidelijke en volledige (zowel schriftelijke als mondelinge) informatie ontvangen over de bijwerkingen die zich kunnen voordoen bij een behandeling met biologicals. - Patiënten vinden het belangrijk dat, als zij bijwerkingen ervaren, duidelijk is tot wie zij zich moeten richten, dus tot de huisarts of de medisch specialist. - Patiënten vinden het belangrijk dat, als zij bijwerkingen ervaren, hier serieus naar wordt gekeken en deskundig op wordt geacteerd. - Patiënten vinden het belangrijk dat zij instructies ontvangen wat zij zelf kunnen doen om bepaalde bijwerkingen te voorkomen. |
Overweging vanuit het patiëntenperspectief bij UV 4: - Patiënten vinden het belangrijk dat zij informatie ontvangen over de het risico op kanker bij biologicals. - Patiënten vinden het belangrijk dat zij actief worden gevolgd op het mogelijk ontstaan van kanker. |
ZWANGERSCHAP EN BIOLOGICALS: |
Overweging vanuit het patiëntenperspectief bij UV 5: Op basis van de focusgroep zijn geen overwegingen aan te dragen. |
BIOLOGICALS EN (OPERATIEVE) INGREPEN: |
Overweging vanuit het patiëntenperspectief bij UV 6: - Patiënten vinden het belangrijk dat de voorschrijvend specialist betrokken is bij het besluitvormingsproces van een operatie. Daarbij is het essentieel dat er direct contact is tussen de betrokken specialisten. - Patiënten vinden het belangrijk dat zij in bezit zijn van een ‘kaartje’ waarop staat dat zij biologicals gebruiken en dat met de specialist contact opgenomen moet worden in geval van tandheelkundige of operatieve ingrepen. - Patiënten vinden het belangrijk dat zij informatie ontvangen over de stappen die gezet moeten worden bij het staken of doorgaan van biologicals bij een operatie. Hierdoor zijn zij in staat zelf actief mee te werken en hebben meer het gevoel controle te hebben over hun behandeling met biologicals. |
FOLLOW-UP VAN DE BEHANDELING MET BIOLOGICALS: |
Overweging vanuit het patiëntenperspectief bij UV 7: - Patiënten vinden het belangrijk dat zij regelmatig (om de 3 tot 6 mnd) door de medisch specialist worden onderzocht waarbij de werking van de biologicals in kaart wordt gebracht. - Patiënten vinden het belangrijk dat zij worden geinformeerd over de uitslag van de periodieke controle zodat zij deelgenoot zijn van het zorgproces. - Patiënten geven aan geconfronteerd te worden met een veelheid aan informatiestromen die regelmatig tegenstrijdig zijn. Zij vinden het belangrijk dat hier meer regie over gevoerd gaat worden. - Patiënten vinden het belangrijk dat professionels aangeven wanneer men geen duidelijkheid ten aanzien van bepaalde vraagstukken kunnen geven omdat nog zoveel onbekend is bij de behandeling van biologicals. - Patiënten vinden het belangrijk regelmatig contact te hebben met de (specialistisch) verpleegkundige zodat zij eventuele vragen kan beantwoorden. |
BIOLOGICALS EN VACCINATIE: |
Overweging vanuit het patiëntenperspectief bij UV 8: - Patiënten vinden het belangrijk dat zij (tijdig) informatie ontvangen over welke vaccinaties zij toegediend kunnen krijgen. - Patiënten vinden het belangrijk dat zij informatie ontvangen bij welke verschijnselen, nadat zij een vaccinatie hebben ontvangen, zij contact op moeten nemen met de medisch speicalist. |
DE BEHANDELING MET BIOLOGICALS: |
Overweging vanuit het patiëntenperspectief bij UV 9: - Patiënten vinden het belangrijk dat de arts door wie zij worden behandeld deskundig is en over de meest recente inzichten beschikt zodat zij erop kunnen vertrouwen in goede handen te zijn. - De (voorschrijvende) medisch specialist dient de regie in handen te houden en daarbij is het overleg met de andere betrokken professionals belangrijk. - Het is belangrijk dat de professionals communicatief zijn en duidelijk uitleg kunnen geven op niveau van de leek. Daarnaast is het wenselijk dat de medisch specialist toegankelijk en laagdrempelig is bij vragen; te weten via de telefoon of email. - Als het niet goed gaat met de patiёnt is het belangrijk dat de medisch specialist confronterend en direct is door aan te geven dat het helemaal niet goed gaat, dat de patient zich overvraagt of dat bijvoorbeeld gestopt moet worden met werken. Het is daarbij belangrijk dat de patiënt geen ruimte wordt gegeven om te marchanderen. |
LANGDURIG VERBLIJF ELDERS: |
Overweging vanuit het patiëntenperspectief bij UV 10: - Patiënten vinden het belangrijk dat zij informatie ontvangen over: - hoe zij de biologicals het beste naar het buitenland kunnen vervoeren; - naar welke gebieden zij kunnen reizen; - de mogelijkheden om in het buitenland een infuus met biologicals te ontvangen.
|
Methode ontwikkeling
Evidence based
Implementatie
Tijdens de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn en de uitvoerbaarheid van de aanbevelingen. Daarbij is gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. De richtlijn is verspreid onder alle relevante beroepsgroepen en instellingen. Een samenvatting van de richtlijn is gepubliceerd in het Nederlands Tijdschrift voor Geneeskunde en in tijdschriften van de deelnemende wetenschappelijke verenigingen.
Werkwijze
De werkgroep heeft een jaar aan de totstandkoming van de richtlijn gewerkt. Binnen de werkgroep was een schrijverscollectief ingesteld. De leden van het schrijverscollectief zochten systematisch naar literatuur en beoordeelden kwaliteit en inhoud ervan. Vervolgens schreven zij een concepttekst waarin de literatuur werd verwerkt. Tijdens vergaderingen lichtten zij hun teksten toe aan de overige leden van de werkgroep. De conceptrichtlijn is in februari 2010 schriftelijk aan alle betrokken wetenschappelijke verenigingen aangeboden en gevraagd de richtlijn aan hun leden voor te leggen. Daarnaast is de richtlijn ook naar wetenschappelijke verenigingen gestuurd die niet in de werkgroep hebben geparticipeerd, te weten oogartsen, neurologen, gynaecologen en tandartsen. De ontvangen commentaren zijn, waar relevant bevonden, verwerkt in de definitieve richtlijn.
Wetenschappelijke onderbouwing
De onderbouwing van de richtlijn is mede gebaseerd op bewijs uit gepubliceerd wetenschappelijk onderzoek. Relevante artikelen werden gezocht met systematische zoekacties. Er werd gezocht tussen 1998 en 2009 in Medline en Embase. Voor de oriënterende search werd ook gezocht in de Cochrane Library en werd specifiek gezocht naar al bestaande richtlijnen in online raadpleegbare (inter)nationale guideline clearinghouses.
Hierbij werd de taal gelimiteerd tot Nederlands, Engels, Duits en Frans. Daarnaast werden artikelen geëxtraheerd uit referentielijsten van opgevraagde literatuur. Dit leverde bij enkele uitgangsvragen nog aanvullende artikelen op.
Doordat de uitgangsvragen niet gericht waren op het beoordelen van de effectiviteit van de interventies maar veelal gingen over bijwerkingen, complicaties en diagnostiek bleek een beperking tot systematische reviews en RCTs vaak niet zinvol. De searches zijn verricht in mei en juni 2009. Voor alle uitgangsvragen is gebruik gemaakt van een uniforme formulering van de patiëntencategorie en de interventie.
Voor de gehanteerde zoektermen wordt verwezen naar Appendix 1. Op verzoek zijn de volledige zoekstrategieën beschikbaar. Daarnaast werden artikelen geëxtraheerd uit referentielijsten van opgevraagde literatuur en zijn enkele relevante publicaties tot 1 november 2009 meegenomen. Lopend onderzoek is buiten beschouwing gelaten. Abstracts van congressen van de afgelopen 2 jaar (november 2007 tot 1 november 2009) zijn meegenomen bij de selectie van de literatuur. Relevante informatie vanuit deze abstract wordt uitgewerkt bij de overige overwegingen. Onder samenvatting van de literatuur / conclusies worden alleen gepubliceerde onderzoeken / richtlijnen uitgewerkt.
De geselecteerde artikelen zijn beoordeeld op kwaliteit van het onderzoek en gegradeerd naar mate van bewijs. Hierbij is de standaardindeling gebruikt: zie tabel 1. Na selectie bleven de artikelen over die als onderbouwing bij de verschillende conclusies staan vermeld. De beoordeling van de verschillende artikelen is opgenomen onder het kopje ‘samenvatting van de literatuur’. Het wetenschappelijk bewijs is vervolgens kort samengevat in een ‘conclusie’. De belangrijkste literatuur waarop deze conclusie is gebaseerd staat bij de conclusie vermeld, inclusief de mate van bewijs (zie tabel 2).
Voor het formuleren van een aanbeveling zijn, naast het wetenschappelijk bewijs, vaak nog andere aspecten van belang, bijvoorbeeld patiëntenvoorkeuren, kosten, beschikbaarheid of organisatorische aspecten. Deze aspecten worden, voor zover niet wetenschappelijk onderzocht, vermeld onder het kopje ‘overwegingen’. In de overige overwegingen spelen de ervaring en de mening van de werkgroepleden een belangrijke rol. De ‘aanbeveling’ is het resultaat van de combinatie van het beschikbare bewijs en de overige overwegingen.
Voor een aantal uitgangsvragen zijn evidencetabellen gemaakt en deze zijn te raadplegen in Appendix 3.
Tabel 1: Indeling van methodologische kwaliteit van individuele studies
|
|
Interventie |
Diagnostische accuratesse onderzoek |
Schade of bijwerkingen, etiologie, prognose* |
|
A1 |
Systematische review van ten minste twee onafhankelijk van elkaar uitgevoerde onderzoeken van A2-niveau |
||
|
A2 |
Gerandomiseerd dubbelblind vergelijkend klinisch onderzoek van goede kwaliteit van voldoende omvang |
Onderzoek ten opzichte van een referentietest (een ‘gouden standaard’) met tevoren gedefinieerde afkapwaarden en onafhankelijke beoordeling van de resultaten van test en gouden standaard, betreffende een voldoende grote serie van opeenvolgende patiënten die allen de index- en referentietest hebben gehad |
Prospectief cohortonderzoek van voldoende omvang en follow-up, waarbij adequaat gecontroleerd is voor ‘confounding’ en selectieve follow-up voldoende is uitgesloten |
|
B |
Vergelijkend onderzoek, maar niet met alle kenmerken als genoemd onder A2 (hieronder valt ook patiënt-controleonderzoek, cohort-onderzoek) |
Onderzoek ten opzichte van een referentietest, maar niet met alle kenmerken die onder A2 zijn genoemd |
Prospectief cohortonderzoek, maar niet met alle kenmerken als genoemd onder A2 of retrospectief cohortonderzoek of patiënt-controleonderzoek |
|
C |
Niet-vergelijkend onderzoek |
||
|
D |
Mening van deskundigen |
||
* Deze classificatie is alleen van toepassing in situaties waarin om ethische of andere redenen gecontroleerde trials niet mogelijk zijn. Zijn die wel mogelijk dan geldt de classificatie voor interventies.
Tabel 2: Niveau van bewijs van de conclusie
|
Conclusie gebaseerd op |
|
|
1 |
Onderzoek van niveau A1 of ten minste twee onafhankelijk van elkaar uitgevoerde onderzoeken van niveau A2 |
|
2 |
Eén onderzoek van niveau A2 of ten minste twee onafhankelijk van elkaar uitgevoerde onderzoeken van niveau B |
|
3 |
Eén onderzoek van niveau B of C |
|
4 |
Mening van deskundigen |
Deze (concept)richtlijn is opgesteld aan de hand van het Appraisal of Guidelines for Research & Evaluation (AGREE) instrument. Dit instrument is in een Europees verband opgesteld om de procedurele kwaliteit van richtlijnen te kunnen beoordelen. Door de aspecten van AGREE te verwerken in de inleiding van de richtlijn, wordt duidelijk aan welke kwaliteitseisen is voldaan.
